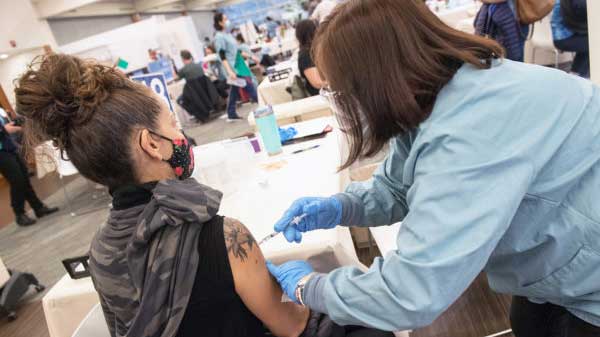
Η Pfizer έλαβε πλήρη έγκριση την Πέμπτη για το χάπι COVID-19 Paxlovid, το οποίο αποτελεί τη βασική θεραπεία κατά του κορονοϊού.
Περισσότερες από 11 εκατομμύρια συνταγές για το Paxlovid έχουν χορηγηθεί από τότε που η Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ επέτρεψε την επείγουσα χρήση στα τέλη του 2021. Το καθεστώς έκτακτης ανάγκης βασίστηκε σε πρώιμες μελέτες και προοριζόταν να είναι προσωρινό εν αναμονή της έρευνας παρακολούθησης.
Ο FDA χορήγησε πλήρη έγκριση για ενήλικες με COVID-19 που αντιμετωπίζουν υψηλό κίνδυνο σοβαρής νόσου, η οποία μπορεί να οδηγήσει σε νοσηλεία ή θάνατο. Αυτή η ομάδα περιλαμβάνει συνήθως ηλικιωμένους και άτομα με παθήσεις όπως ο διαβήτης, το άσθμα και η παχυσαρκία.
Η αμερικανική κυβέρνηση έχει αποθηκεύσει εκατομμύρια δόσεις του Paxlovid και οι ασθενείς θα συνεχίσουν να το λαμβάνουν δωρεάν, ανέφερε ο FDA σε ανακοίνωσή του. Περισσότερα από 14.000 νέα κρούσματα COVID-19 αναφέρονταν κάθε εβδομάδα τον περασμένο μήνα, αν και τα περισσότερα κρούσματα στις ΗΠΑ δεν αναφέρονται πλέον στις υγειονομικές αρχές.
Το Paxlovid είναι το τέταρτο φάρμακο για το COVID-19 που λαμβάνει πλήρη έγκριση από τον FDA και το πρώτο σε μορφή χαπιού. Οι μέχρι τώρα εγκεκριμένες θεραπείες είναι ενδοφλέβια ή ενέσιμα φάρμακα, τα οποία συνήθως χορηγούνται σε κλινικές ή νοσοκομεία.
Η Pfizer μελέτησε αρχικά το Paxlovid στους ασθενείς με τον υψηλότερο κίνδυνο COVID-19: ανεμβολίαστους ενήλικες με άλλα προβλήματα υγείας και χωρίς ενδείξεις προηγούμενης λοίμωξης από κορονοϊό. Σε αυτή την ομάδα, ο FDA δήλωσε ότι το φάρμακο μείωσε τον κίνδυνο νοσηλείας ή θανάτου κατά 86% όταν χορηγήθηκε λίγο μετά την εμφάνιση των συμπτωμάτων.
Καθώς το Paxlovid άρχισε να χρησιμοποιείται ευρέως το 2021, γιατροί και ασθενείς ανέφεραν περιπτώσεις συμπτωμάτων του COVID-19 που επέστρεφαν αρκετές ημέρες μετά τη θεραπεία με το φάρμακο. Αλλά ο FDA δήλωσε την Πέμπτη ότι «δεν υπάρχει σαφής συσχέτιση», μεταξύ του φαρμάκου της Pfizer και των περιπτώσεων αναζωπύρωσης.
Το συμπέρασμα αυτό υποστηρίχθηκε από μια ανεξάρτητη ομάδα συμβούλων του FDA, η οποία ψήφισε υπέρ της σύστασης της πλήρους έγκρισης του φαρμάκου σε συνεδρίαση νωρίτερα φέτος.
Με πληροφορίες από ASSOCIATED PRESS


![[300,399] Ψιχάλες](https://openweathermap.org/img/wn/04n@2x.png)